Die Wollemie (Wollemia nobilis) und eine offene Frage
Artikelinhalt
- Ein kurzes Portrait der Wollemie und die Geschichte ihrer Entdeckung
- Präparation
- Verwendete Technik
- Der Spross unter dem Mikroskop
- Das Blatt unter dem Mikroskop
- "Compartemented Cells" - eine Besonderheit der Araukariengewächse
- Auffälligkeiten im Phloem und Calciumoxalatablagerungen
- Fazit
- Nachtrag 1: nach weiteren Untersuchungen in Darmstadt (08.04.2017)
- Nachtrag 2: Nacréwände - das Rätsel ist gelöst!
- Dank
- Literatur und Links
- Bildquellen
Ein kurzes Portrait der Wollemie und die Geschichte ihrer Entdeckung

Bild 1: Wollemien aus der Luft: zwei ausgewachsene Pflanzen an einem der Standorte im Wollemi-Nationalpark
Die rissige Rinde der ausgewachsenen Pflanze ist dunkelbraun, harzig und von rundlichen Erhebungen bedeckt. Der junge Spross trägt mit Beginn des sekundären Dickenwachstums eine glatte hellbraune Rinde mit deutlichen Blattnarben. Die Zweige hingegen bleiben grün. Sie sind an ihrem Ansatzpunkt am Stamm von einer konischen Hülle umgeben, in deren unterem Bereich die Sollbruchstelle zu erkennen ist, an der der Ast später abgeworfen wird, wenn er zu alt (zu schwer ...) geworden ist (Bild 5). [1] & [2]

Bild 6: Abgeworfener zweijähriger Zweig von der schattigen Rückseite der Pflanze aus Bild 2. Auffällig sind die im zweiten Jahr (Wachstumsabschnitt) links stark vergrößerten Blätter. Offensichtlich hat die Anstrengung aber nicht ausgereicht, um im Schatten sinnvoll Photosynthese betreiben zu können.
Die männlichen Zapfen sind bei einer Dicke von ca. 3 cm etwa 7 bis 9 cm lang und tragen gelblichbraune Microsporophyllen, die im unreifen Zustand auf dem Zapfen ein fest geschlossenes Rautenmuster bilden.
Um das natürliche Vorkommen zu schützen, entschloss sich die Nationalparkverwaltung, die Wollemie mit einem Partner aktiv zu vermarkten und so "Raubexpeditionen" möglichst unattraktiv zu machen. Dazu hat der Botanische Garten Sydney ein Forschungs- und Erhaltungsprogramm gestartet, in dessen Rahmen mit verschiedenen Methoden Jungpflanzen gezüchtet werden. Am 23.10.2005 erbrachte die Versteigerung einer limitierten Anzahl von 292 Pflanzen der ersten Vermehrungs-Generation bei Sotherby's einen Erlös von 1,5 Millionen USD.
Und so hat z.B. die Firma Kientzler Jungpflanzen GmbH die Markteinführung der Wollemie in Deutschland im Mai 2006 in den Botanischen Gärten der Universität Bonn offiziell vorgestellt und dem Garten ein erstes Exemplar geschenkt.
Kurz zur Präparation
Geschnitten habe ich die frischen Blätter in Möhreneinbettung und den Spross freistehend auf dem Handzylindermikrotom mit Leica Einmalklingen im SHK-Klingenhalter. Die Schnittdicke beträgt rund 60 bzw. 50 µm. Nach einer Schnittfixierung in AFE für ca. 11 bis 16 Stunden wurden die Schnitte in Aqua dest überführt.
Zwischenzeitlich habe ich jeweils auch einige Aufnahmen von den frischen Schnitten gemacht.
Anschließend habe ich die Schnitte dann für etwa zwei Minuten mit Klorix (1:4 in Aqua dest. als Ersatz für Eau de Javelle) behandelt und nach sehr gutem Ausspülen für rund 12 bis 22 Stunden mit Chloralhydrat gebleicht (250g auf 100ml Aqua dest.). Danach war wieder gründliches Spülen angesagt.
Nach dieser recht aufwändigen Vorbereitung wurde dann mit Dujardin Grün nach Rolf-Dieter Müller gefärbt.
Eingedeckt sind die Schnitte - nach gründlichem Entwässern in reinem Isopropanol - in Euparal.
Weitere Informationen zur Erstellung botanischer Dauerpräparate finden Sie auf der zugehörigen Themenseite.
Die verwendete Technik
Alle Mikroaufnahmen sind mit Zerene Stacker V1.04 (64bit) gestackt. Die anschließende Nachbereitung beschränkt sich auf die Normalisierung und ein leichtes Nachschärfen nach dem Verkleinern auf die 1024er Auflösung (alles mit XNView in der aktuellen Version). Bei stärker verrauschten Aufnahmen lasse ich aber auch mal Neat Image ran.
Der Spross unter dem Mikroskop
Bilder 14a-d: Ungefärbte Schnitte vom zweijährigen Spross
Bilder 15a,b: Mit Dujardin Grün gefärbte Schnitte vom zweijährigen Spross
Wie später im Blatt sehen wir zahlreiche Sekretgänge (SG) mit ihrem innen liegenden Drüsenepitel (DEp) sowohl im Spross als auch im Blatt. Sklerifizierten Idioblasten und die sklerenchymatischen Fasern oberhalb des Phloems sind ebenfalls zu entdecken.
Bilder 16a-d: Xylem, Cambium und Phloem vom zweijährigen Spross
Besonders in den Bildern 16c & d sehen wir deformierte Phloemzellen, sie werden uns im Blatt wieder begegnen. Im Bild 16d sind einige besonders schöne Exemplare mit Pfeilen gekennzeichnet
Der Blattansatz zeigt die selbe Anatomie wie später die Querschnitte der Blätter selbst:
Bilder 17a,b: Detailaufnahme vom Blattansatz
Um das Bild abzurunden, folgt ein genauerer Blick auf eine Blattspur und das Markparenchym:
Bilder 18a-d: Detailaufnahme vom Blattansatz
Das Blatt unter dem Mikroskop
Nun aber zu den Schnitten! Zur Übersicht hier noch einmal eine Wiederholung des Bildes 13 mit der Schnittführung:
Bilder 22a-d: Blattrand eines vierjährigen Blattes von Wollemia nobilis im Querschnitt
Eingelagert im Schwammparenchym finden wir zum einen große Sekretgänge, an deren Wänden innen ein Drüsenepitel zu finden ist. Bei den frischen Schnitten finden sich über den ganzen Schnitt verteilt kleine ölige Tröpfchen. Ich vermute, dass es sich dabei um den Inhalt der Sekretgänge handelt, der beim Schneiden ausgetreten ist. Zum anderen liegen hier aber auch die parallel verlaufenden kollateralen Leitbündel.
An der Blattunterseite finden wir dann wieder die Hypodermis und die Epidermis mit ihrer Cuticula, diesmal unterbrochen von zahlreichen Stomata in unterschiedlichster Orientierung. Leider habe ich von den an der Blattoberseite liegenden Stomata keines erwischt.
Bleibt zu erwähnen, dass sowohl die Cuticula als auch die Hypodermis am Blattrand besonders stark ausgeprägt sind.
Bilder 23a-d: Quer- und Längsschnitt in der Fläche des vierjährigen Blattes
Im Längsschnitt erkennen wir die gleiche Abfolge, da hier eines der Leitbündel getroffen ist. Schön auch die Hoftüpfel der Tracheen (Ht), das oberhalb des Xylems verlaufende dunkelrote Band scheint ein Färbeartefakt (Art) zu sein.
Bilder 24a-h: Leitbündel und Palisadenparenchym des vierjährigen Blattes im Detail
Im Längsschnitt zunächst noch einmal die Hoftüpfel der Tracheen (24f & g) sowie Siebfelder mit Siebplatten als Verbindung zwischen den Siebzellen (SP).
Schauen wir uns nun noch ein wenig in den Querschnitten um und beginnen mit der Cuticula am Blattrand:
Bilder 25a,b: Blattrand mit ausgeprägter Cuticula
Am unteren Rand ein angeschnittener Sekretgang mit Drüsenepitel.
Bilder 26a,d: Einer der Idioblasten aus der Nähe
Die folgende animierte GIF-Datei empfindet quasi eine Fahrt durch das Präparat durch Fokussieren mit dem Feintrieb des Mikroskops nach. Es besteht aus den Einzelbildern des Stapels, aus dem die Bilder 26a & b berechnet wurden.
Bilder 28a,b: Stomata an der Blattunterseite des vierjährigen Blattes
"Compartemented Cells" - eine Besonderheit der Araukariengewächse
Eines der Ziele der Arbeit "Leaf Anatomy of Wollemi Pine (Wollemia nobilis, Araucariaceae)" (Burrow & Bullocks, 1999, [3]) war es, die systematische Zuordnung der Wollemie zu untermauern. In der Familie der Arau- kariengewächse (Araucariaceae) gibt es mit der Entdeckung der Wollemie drei Gattungen: Araucaria, Agathis und Wollemia. Wollemia wird dabei näher an der Gattung Araucaria gesehen und hat sich entwicklungsgeschichtlich früher entwickelt als Agathis, die somit die jüngste Gattung in der Familie ist.
Dies leiten die Autoren vom Vorhandensein der Compartemented Cells ab, da diese bei Araucaria und Wollemia vorhanden sind, nicht aber bei Agathis.
Für die Araukarien haben Mastroberti und de Araujo Mariath diesen speziellen Zelltyp genauer beschrieben [4] & [5]. Die erste korrekte Beschreibung geht jedoch schon auf Bamber et al. (1978) zurück, während sie Barsali (1909) noch als große Interzellularräume interpretiert hat.
Große Interzellularräume bzw. große Zellen mit dünnen Zellwänden im Schwammparenchym? Das kennen wir auch von den hier gezeigten Schnitten, z.B. im Bild 22d:
Die Compatemented Cells sind Zellen, die ein Pektin produzieren und einlagern, bis das gesamte Lumen der Zelle damit gefüllt ist. Dann sterben sie ab. Dabei erhält die Pektinschleim-Füllung eine Struktur, die an eine Unterteilung des Zellinneren erinnert, daher der Name. ([4], S. 269, Fig. 5 & [3], S. 801, Fig. 5). Da diese Zellen einen sehr großen Raum im Mesophyll einnehmen, müssen sie für die Araukarien einen großen Vorteil gebracht haben. Vermutet wird eine Funktion als Wasser- und/oder Stoffwechselprodukt-Speicher.
So, und wo sind diese Zellen mit ihrer seltsamen Schleimfüllung nun in meine Schnitten? Ich hab sie alle fein säuberlich ausgeputzt ... :)
... wirklich alle? Nein, mit etwas Glück konnte ich in zwei etwas dicker geschnittenen Präparaten einige Zellen finden, auf die die Beschreibung passt und die auch noch Reste der Schleimfüllung enthalten. Die Strukturen, die zum Namen Compartemented Cells geführt haben sind jedoch verschwunden: sicherlich ein Effekt der Behandlung mit Klorix und Chloralhydrat.
Bilder 30a,b: Compartemented Cells im Blattquerschnitt
Bilder 31a-c: Compartemented Cells im Detail
Auffälligkeiten im Phloem und Calciumoxalatablagerungen
Interessant ist auch, dass es in den mir vorliegenden Aufsätzen zu Blattanatomie von Wollemia nobilis keinen entsprechenden Hinweis gibt ([3] und [5]). Zu erwarten wäre gemäß dieser Arbeiten ein normal gebildetes Phloem, typischerweise nur mit Siebzellen, das über ein Cambium jährlich neu gebildet wird (die Wollemie hat in den Blättern also offen kollaterale Leitbündel). Altes, disfunktionales Phloem zeigt sich dann halbmondförmig zusammengepresst und an der Endodermis anliegend am unteren Rand des Leitbündels ([3], S. 801, Fig. 6).
![Bild 32: Fig. 6 aus dem Artikel 'Leaf Anatomy of Wollemi Pine (Wollemia nobilis, Araucariaceae)' von Geoffrey E. Burrows and Suzanne Bullock [3]. Der rote Pfeil markiert das halbmondförmig zusammengeschobene disfunktionale Phloem (cp) am unteren Rand eines Leitbündels im Blatt von Wollemia nobilis. Bild 32: Fig. 6 aus dem Artikel 'Leaf Anatomy of Wollemi Pine (Wollemia nobilis, Araucariaceae)' von Geoffrey E. Burrows and Suzanne Bullock [3]. Der rote Pfeil markiert das halbmondförmig zusammengeschobene disfunktionale Phloem (cp) am unteren Rand eines Leitbündels im Blatt von Wollemia nobilis.](../../_pics/8675/170114_Wollemia_nobilis_Blatt_quer_Leitbuendel_Burrows_3_600.jpg)
Bild 32: Fig. 6 aus dem Artikel 'Leaf Anatomy of Wollemi Pine (Wollemia nobilis, Araucariaceae)' von Geoffrey E. Burrows and Suzanne Bullock [3]. Der rote Pfeil markiert das halbmondförmig zusammengeschobene disfunktionale Phloem (cp) am unteren Rand eines Leitbündels im Blatt von Wollemia nobilis.
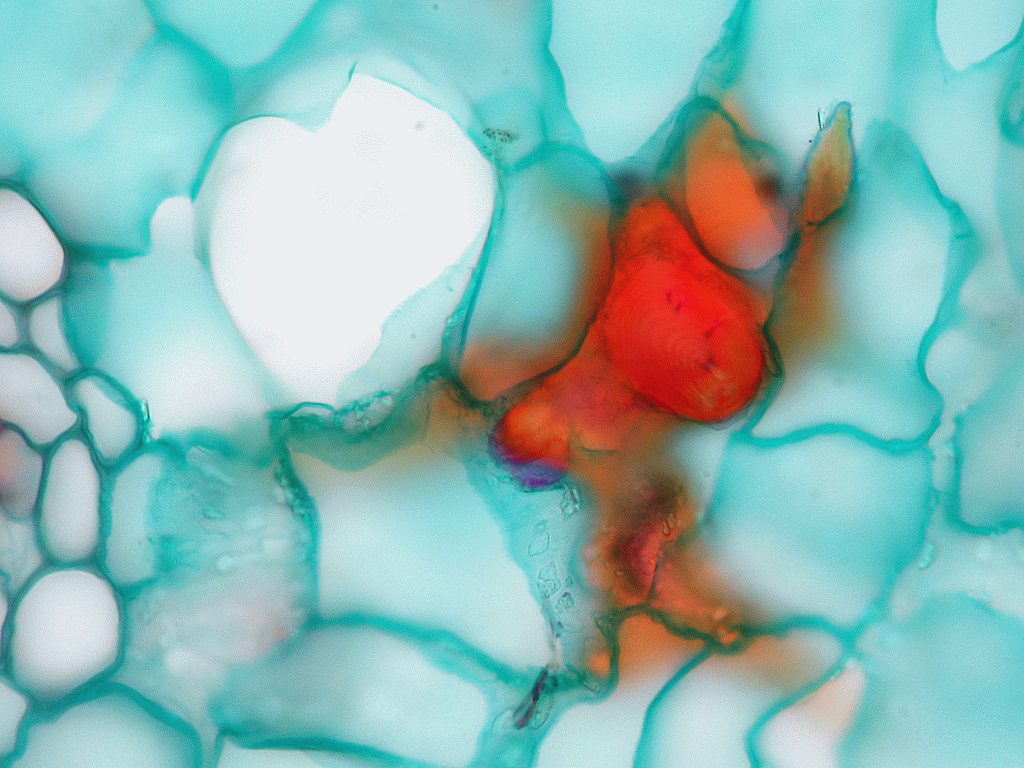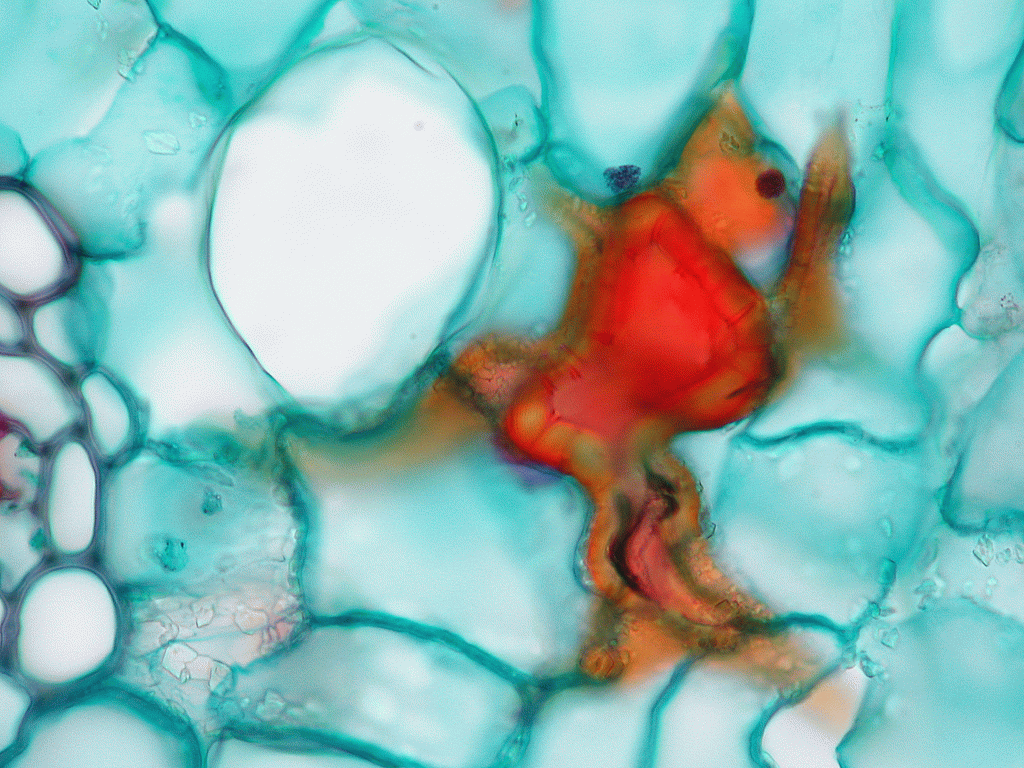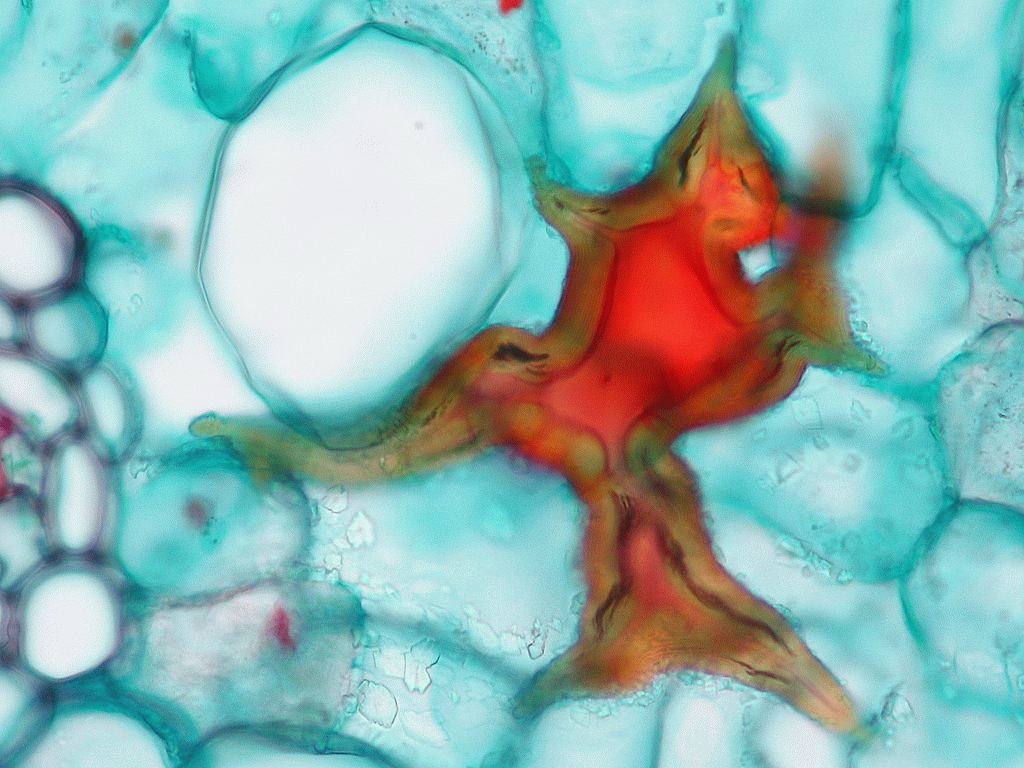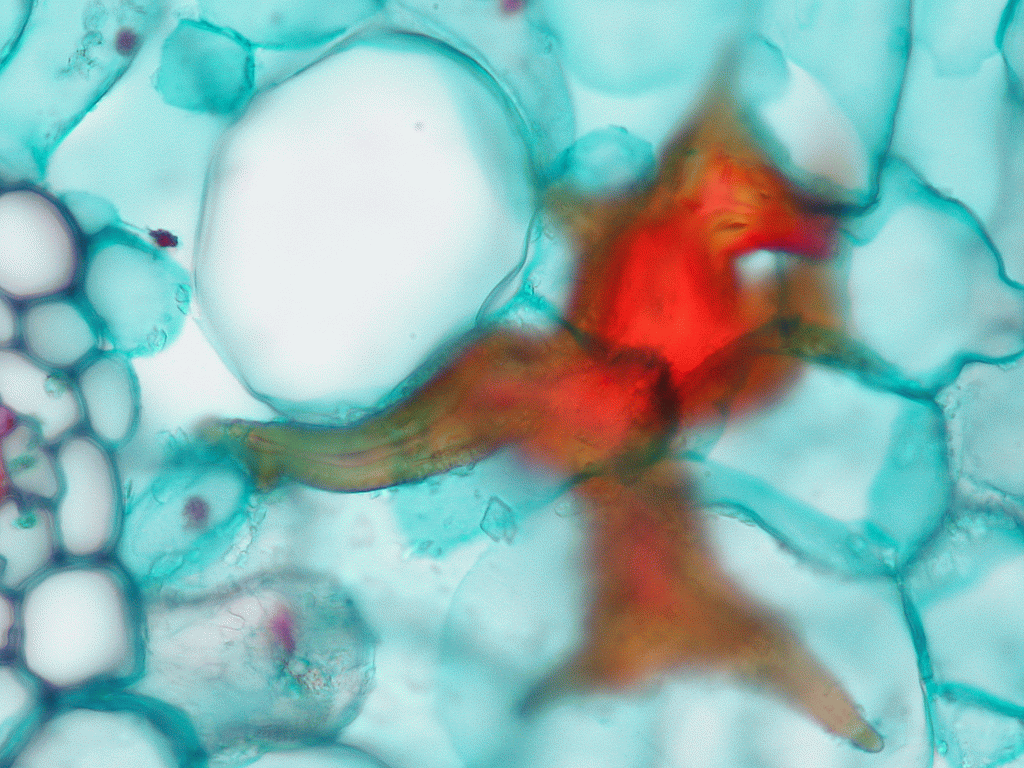
Zum Einstieg noch einmal ein Leitbündel aus dem vierjährigen Blatt als Vergleichsmaßstab. Die Bilder zeigen schön die deformierten Zellen, die entgegen der Situation in Bild 32 über das ganze Phloem verteilt liegen. Der Halbmond ist nicht zu erkennen und im Phloem selbst gibt es einige Stränge scheinbar funktionaler Siebzellen:

Bild 33: Unser Referenzleitbündel vom vierjährigen Blatt in Dujardin Grün Färbung; Vergrößerung 400x, Stapel aus 12 Bildern
Bilder 34a-h: Schnitte vom einjährigen Blatt
Besonders die Bilder mit eintausendfacher Vergrößerung (34g & h) zeigen uns aber etwas vom genauen Aufbau der disfunktionalen Zellen: wir sehen in dunklem Blau die Zellmembran, die von der aufgequollenen Zellwand quasi nach innen zusammen geschoben und eingefaltet wurde. Allerdings ist das Lumen der betroffenen Siebzellen hier (noch?) nicht ganz geschlossen.
Was haben wir gelernt: Ein Artefakt scheidet wahrscheinlich aus, da die ungefärbten Schnitte sich genau so darstellen, wie die mit Dujardin Grün gefärbten. Ausserdem gibt es im einjährigen Blatt sowohl Leitbündel mit gut durchlässigem als auch mit annähernd vollständig zugequollenem Phloem.
Versuchen wir also zur Sicherheit noch einmal eine sanftere Präparation ohne Bleiche und mit W3Asim II Färbung und nehmen mehr Leitbündel des Querschnitts unter die Lupe:
Bilder 35a-n: Schnitte vom zweijährigen Blatt
An diesem Punkt habe ich Herrn Dr. Geoffrey E. Burrows, einen der Autoren des Artikels zur Blattanatomie der Wollemie [3] angeschrieben, und ihm meine Funde vorgestellt. Er hat zunächst noch einmal frische Schnitte von der Wollemie aus seinem Garten gemacht, die aber den gleichen Leitbündelaufbau wie in seinem Artikel zeigten (siehe Bild 32). Auch er hatte keine Erklärung für das weitestgehend disfunktionale Phloem in den Blättern der Bonner Pflanze.
Exkurs: Die unterschiedlich alten Blätter boten jedoch auch eine gute Gelegenheit, einmal zu schauen, wie es sich mit der Ablagerung des Calciumoxalats verhält:
Bilder 36a-h: Calciumoxalatablagerungen abhängig vom Alter des Blattes
Wie schon weiter oben beschrieben, enthält auch die mittlere Schicht der Cuticula eingelagerte Calciumoxalatkristalle. Diese sind aber bereits am Ende der ersten Wachstumsperiode, hier beim einjährigen Blatt vorhanden und bleiben in den späteren Jahren unverändert.
Fazit
- Sowohl im Phloem des Sprosses als auch in dem der Blätter finden wir bei Wollemia nobilis einen sehr großen Anteil disfunktionaler Siebzellen, die wie zugequollen wirken. Der Effekt beruht auf stark verdickten Zellwänden der Phloemzellen, ohne dass z.B. eine Sklerifizierung vorliegen würde.
- In den Blättern sind die äußeren der 8 bis 9 parallelen Leitbündel durchlässiger als die in der Mitte, aber alle Leitbündel haben im Phloem auch durchlässige Siebzellen.
- Aussehen und Anordnung des Phloems widerspricht den Beschreibungen in den einschlägigen Artikeln (siehe insbesondere Bild 32 und [3])
- Eine Präparationsartefakt konnte durch die Betrachtung frischer Schnitte und einer alternativen Färbung ausgeschlossen werden.
- Die Deformation ist unabhängig vom Alter der Blätter (Eingeflossen sind die Ergebnisse von Schnitten durch Blätter im Alter von einem, zwei und vier Jahren)
- Zeitpunkt der Probenahme war Mitte Oktober, also am Ende der Wachstumsperiode
Nach Diskussion mit Dr. Detlef Kramer besteht die Möglichkeit, dass es sich hier um eine reversible Veränderung zum Schutz vor Feuchtigkeitsverlust und Erfrierungen in der kalten Jahreszeit handelt. Was bedeutet, dass Blätter aller Altersstufen mit Beginn der neuen Wachstumsperiode im Frühjahr wieder ein normales Phloem zeigen müssten.
Alternativ kommt eine krankhafte Veränderung oder eine Veränderung aufgrund eines ungünstigen Standorts in Betracht.
Dies lässt sich einfach prüfen: im kommenden Frühjahr werde ich noch einmal Proben von den Bonner Wollemien untersuchen und auch schauen, wie es sich bei den Wollemien im Botanischen Garten der TU Darmstadt verhält. Ich hoffe, dann eine Lösung zu finden oder wenigstens eine der Theorien erhärten zu können und werde wieder berichten.
Nachtrag auf Basis weiterer Untersuchungen vom 08.04.2017
Die minimalen Einwirkzeiten führet allerdings zu Präparationsartefakten vom nicht gänzlich entfernten Harz aus den großen Harzgängen, die sich auch in den Bildern der Schnitte wieder finden.
Bilder 38a-c: Präparation der Blätter im Rahmen des Workshops auf der Kornrade 14

Bild 39: Das Phloem der Darmstädter Pflanzen zeigt die gleichen Deformationen wie bei den Bonner Proben, Vergrößerung 400x
Bilder 40a-c: Übersicht und Details
Wie ist das zu deuten? Eine krankhafte Veränderung kann meines Erachtens ausgeschlossen werden, da sie über alle beprobten Pflanzen sehr unwahrscheinlich ist. Was bleibt, wäre eine Schutzreaktion der Siebzellen in der Ruhephase, die mit Beginn der nächsten Wachstumsphase zurück gebildet wird.
Dazu war es diesmal noch zu früh, ich werde also ab Mitte Mai noch mal Proben in Bonn nehmen und auch die Kollegen aus Darmstadt wollen dann noch einmal schauen.
Bilder 41a,b: Transfusionstracheiden in der Blattspitze der Wollemie
Alles in allem ein weiterer Cliffhanger, Ende Mai lesen wir uns - hoffentlich - wieder.
Nachtrag vom 24.09.2017: Nacréwände - das Rätsel ist gelöst!
Kurz und knapp: die verdickten Zellwände zeigten sich wie in allen anderen Funden bisher auch in den Siebelementen dieser Proben. Die Theorie, dass die Zellwandverdickungen eine Schutzfunktion in der Ruhephase sein könnten, war somit klar widerlegt.
Bilder 42a,e: Bilder vom frischen Austrieb der Wollemien in Bonn

Bild 43: Auch im Phloem der noch nicht ausdifferenzierten Blätter zeigen die Siebelemente die bekannten Wandverdickungen ... und nun?
Und siehe da, dort wird man z.B. bei Esau auf der Seite 206 in einem kleinen Abschnitt mit der Überschrift "Wandstruktur" fündig. Es ist die Rede von der Nacréwand (franz. perlmuttartig glänzend), die so dick sein kann, dass sie das Zelllumen verstopft. Seinerzeit (1969) war das Thema wohl noch recht neu, es wurde zumindest für die Abietoidae unter den Coniferales angenommen, dass es sich um eine echte Sekundärwand handelt.
Soweit ganz kurz und knapp aus dem Esau ... zu "perlmuttartig" passt sehr gut das folgende Bild vom frischen Schnitt eines zweijährigen Blattes:

Bild 44: Leitbündel eines frischen Schnittes. Die Siebelemente erscheinen perlmutartig gefärbt - handelt es sich um Nacréwände?
In den Siebzellen der Farnpflanzen kann die Zellwand stark anschwellen, so dass das Zelllumen fast verschwindet. Solche Zellwände haben im Lichtmikroskop Perlmuttglanz, man bezeichnet sie als Nacré-Wandschichten (Abb. 5.8). Die Nacréwand stellt nur ein Übergangsstadium dar, denn im ausdifferenzierten Zustand besitzen die Siebzellen der Pteridophyten kaum dickere Zellwände als die Parenchymzellen (Warmbrodt 1980, Evert 1984).
In Coniferennadeln, die mehrere Jahre funktionsfähig bleiben (Picea abies), behalten die Siebzellen des sekundären Phloems ihre Nacréwände bis zu Obliteration (Blechschmidt u. Huber 1952). Dickwandige, obliterierte (= abgestorbene, Anm. des Autors) Siebelemente bilden den Knorpelbast (Holdheide u. Huber 1952), der auch als Hornbast, Hornprosenchym oder Keratenchym bezeichnet wurde (Esau 1969).
Die Aufeinanderfolge cytologischer Veränderungen in den jungen Siebelementen spricht dafür, dass lytische Vorgänge die Funktionsbereitschaft dieser Stoffleitungsbahnen vorbereiten. Offenbar werden nicht mehr benötigte Cytoplasmabestandteile duch das Plasmalemma in die gequollene Zellwand geschleust, dort aufgelöst, mit dem Apoplastwasser entfernt und anderen Geweben nutzbar gemacht. Das Vorkommen von Lomasomen (multivesicular bodies) oder Lysosomen spricht für diesen Ablauf. Für die reifen, ausdifferenzierten Siebelemente ist characteristisch, dass sie im Lichtmikroskop leer erscheinen.
Insbesondere mit Blick auf die Abbildung 5.8 auf Seite 144 aus der Funktionellen Pflanzenanatomie betrachte ich das Rätsel um die aufgequollenen Zellwände der Siebelemente bei Wollemia nobilis damit als gelöst. Nacréwände finden sich also auch bei den Araucariae.
Bild 45: Abb. 5.8 aus Funktionelle Pflanzenanatomie, Eschrich 2004, Seite 144

Bild 45: Abb. 5.8 aus Funktionelle Pflanzenanatomie, Eschrich 2004, Seite 144
Bilder 46a,c: Die Probe aus Australien
Bilder 47a-n: Nacréwände bei Wollemia nobilis
Dank
Many thanks to Dr. Geoffrey E. Burrows for the friendly consideration of my questions and the review of my findings doing slices from the leaves of his own Wollemi Pine. And also for sending a specimen of his tree for analysis and comparison.
Mein Dank gilt auch der Leitung der Botanischen Gärten von Bonn und Darmstadt, mit deren Erlaubnis ich die entsprechenden Proben von den Wollemien an beiden Standorten nehmen konnte.
Literatur und Links
in the Araucariaceae.
W. G. Jones, K. D. Hill & J. M. Allen
Telopea 6, S. 173–176 (1995), ISSN 0312-9764
(Erstbeschreibung)
[2] An Anatomical Assessment of Branch Abscission and Branch-base
Hydraulic Architecture in the Endangered Wollemia nobilis
G. E. Burrows, P. F. Meagher and R. D. Heady, 2006
[3] Leaf Anatomy of Wollemi Pine (Wollemia nobilis, Araucariaceae)
Geoffrey E. Burrows and Suzanne Bullock
Australian Journal of Botany 47(5), 1999, S. 795 - 806
[4] Leaf anatomy of Araucaria angustifolia
(Bertol.) Kuntze (Araucariaceae)
ALEXANDRA A. MASTROBERTI and JORGE E.A. MARIATH
Revista Brasil. Bot., V.26, n.3, p.343-353, jul.-set. 2003
[5] Compartmented cells in the mesophyll of
Araucaria angustifolia (Araucariaceae)
Alexandra A. Mastroberti and Jorge Ernesto de Araujo Mariath
Australian Journal of Botany, 2003, 51, 267–274
[6] Botany for Degree Students - Gymnosperms
Vasishta, Sinha, Kumar, S.Chand Reprint 2016
[7] Wollemia nobilis im Botanischen Garten Bonn
Webseite des Botanischen Gartens Bonn
[8] Botanische Schnitte mit dem Zylindermikrotom
Jörg Weiß, MBK 2011
[9] Dujardin Grün - eine alte Färbung für botanische Schnitte
im neuen Gewand
Dujardin Grün Färbung von Rolf-Dieter Müller, MKB 2011
[10] Tabelle der Abkürzungen zur Pflanzenanatomie
Jörg Weiß, MKB 2011
[11] The Wollemie Pine
James Woodford, 2000
Die Geschichte der Entdeckung der Wollemie
Bildquellen
- Bild 1: Zwei ausgewachsene Wollemien aus der Luft
Geoffrey Burrows und Suzanne Bullock,
aus "Wollemia nobilis, a new living Australian genus
and species in the Araucariaceae" - Bild 3: Polkappe am Haupttrieb von Wollemia nobilis
Aufnahme von Tony Rodd, private Verwendung frei - Bild 10: Männlicher Zapfen von Wollemia nobilis
Aus Wikipedia, User Velela, CC BY-SA 3.0 - Bild 11: Junger weiblicher Zapfen von Wollemia nobilis
Aus photy.org, public domain, Autor nicht angegeben - Bild 12: Reifer weiblicher Zapfen von Wollemia nobilis
Aus http://www.growingontheedge.net von Kev Spence, UK - Bild 32: Leitbündel im Blatt von Wollemia nobilis
Geoffrey Burrows und Suzanne Bullock,
aus "Leaf Anatomy of Wollemi Pine (Wollemia nobilis, Araucariaceae)" - Bild 46: Siebzellen von Farnpflanzen
Zitat aus "Funktionelle Pflanzenanatomie", Eschrich 2004, S. 144 - Alle anderen Aufnahmen vom Autor des Artikels
Zurück zum Artikelanfang Zurück zum Inhaltsverzeichnis